Litijumske baterije imaju prednosti prenosivosti i brzog punjenja, pa zašto onda olovno-kiselinske baterije i druge sekundarne baterije još uvijek kruže na tržištu?
Osim problema troškova i različitih područja primjene, drugi razlog je sigurnost.
Litijum je najaktivniji metal na svetu.Pošto su njegove hemijske karakteristike previše aktivne, kada je metalni litijum izložen vazduhu, on će imati žestoku oksidacionu reakciju sa kiseonikom, pa je sklon eksploziji, sagorevanju i drugim pojavama.Osim toga, redoks reakcija će se također pojaviti unutar litijumske baterije tokom punjenja i pražnjenja.Eksplozija i spontano izgaranje uglavnom su uzrokovani akumulacijom, difuzijom i oslobađanjem litijumske baterije nakon zagrijavanja.Ukratko, litijumske baterije će generisati mnogo toplote tokom procesa punjenja i pražnjenja, što će dovesti do porasta unutrašnje temperature baterije i neujednačene temperature između pojedinih baterija, što će uzrokovati nestabilne performanse baterije.
Nesigurno ponašanje litijum-jonske baterije koja se odgađa od temperature (uključujući prekomjerno punjenje i prekomjerno pražnjenje, brzo punjenje i pražnjenje, kratki spoj, uvjeti mehaničke zloupotrebe, visokotemperaturni termički udar, itd.) vjerovatno će izazvati opasne nuspojave unutar baterije i stvoriti toplinu, direktno oštećujući pasivni film na površini negativne i pozitivne elektrode.
Postoji mnogo razloga za izazivanje termalnih nesreća litijum-jonskih baterija.Prema karakteristikama okidanja, može se podijeliti na okidanje mehaničke zloupotrebe, okidanje električnog zlostavljanja i okidanje toplinske zloupotrebe.Mehaničko zlostavljanje: odnosi se na akupunkturu, ekstruziju i udar teških predmeta uzrokovanih sudarom vozila;Električna zloupotreba: općenito uzrokovana nepravilnim upravljanjem naponom ili kvarom električne komponente, uključujući kratki spoj, prekomjerno punjenje i prekomjerno pražnjenje;Zloupotreba topline: uzrokovana pregrijavanjem uzrokovanom nepravilnim upravljanjem temperaturom.
Ove tri metode pokretanja su međusobno povezane.Mehanička zloupotreba će općenito uzrokovati deformaciju ili pucanje membrane baterije, što će rezultirati direktnim kontaktom između pozitivnog i negativnog pola baterije i kratkim spojem, što rezultira električnom zloupotrebom;Međutim, pod uvjetom zloupotrebe električne energije, stvaranje topline kao što je Joule toplina se povećava, uzrokujući porast temperature baterije, što se razvija u zloupotrebu topline, što dalje pokreće lančanu nuspojavu stvaranja topline unutar baterije i konačno dovodi do pojave topline baterije.
Termički bijeg baterije uzrokovan je činjenicom da je brzina stvaranja topline baterije mnogo veća od brzine disipacije topline, a toplina se akumulira u velikoj količini, ali se ne raspršuje na vrijeme.U suštini, „termički bijeg“ je proces povratnog ciklusa pozitivne energije: porast temperature će uzrokovati da sistem postane vruć, a temperatura će porasti nakon što sistem postane vruć, što će zauzvrat učiniti da sistem postane topliji.
Proces termičkog bijega: kada unutarnja temperatura baterije poraste, SEI film na površini SEI filma se razgrađuje pod visokom temperaturom, litijum ion ugrađen u grafit će reagirati s elektrolitom i vezivom, dodatno povećavajući temperaturu baterije do 150 ℃, a na ovoj temperaturi će se dogoditi nova burna egzotermna reakcija.Kada temperatura baterije dostigne iznad 200 ℃, materijal katode se raspada, oslobađajući veliku količinu toplote i gasa, a baterija počinje da se izboči i neprekidno se zagreva.Anoda ugrađena u litijum počela je da reaguje sa elektrolitom na 250-350 ℃.Napunjeni materijal katode počinje da prolazi kroz burnu reakciju raspadanja, a elektrolit prolazi kroz burnu reakciju oksidacije, oslobađajući veliku količinu toplote, stvarajući visoku temperaturu i veliku količinu gasa, izazivajući sagorevanje i eksploziju baterije.
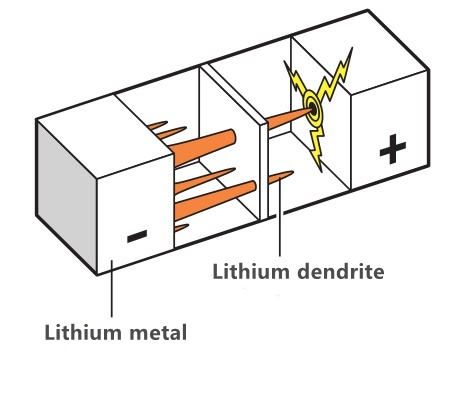
Problem taloženja litijum dendrita tokom prekomernog punjenja: Nakon što je litijum kobalatna baterija potpuno napunjena, velika količina litijum jona ostaje u pozitivnoj elektrodi.To znači da katoda ne može zadržati više litijum jona vezanih za katodu, ali u prenapunjenom stanju, višak litijumovih jona na katodi će i dalje plivati do katode.Budući da se ne mogu u potpunosti zadržati, metalni litijum će se formirati na katodi.Pošto je ovaj metalni litijum dendritski kristal, naziva se dendrit.Ako je dendrit predugačak, lako je probiti dijafragmu, uzrokujući unutrašnji kratki spoj.Kako je glavna komponenta elektrolita karbonat, njegova tačka paljenja i ključanja su niske, pa će izgorjeti ili čak eksplodirati na visokoj temperaturi.
Ako se radi o polimer litijumskoj bateriji, elektrolit je koloidni, koji je sklon žešćem sagorevanju.Kako bi riješili ovaj problem, naučnici pokušavaju zamijeniti sigurnije katodne materijale.Materijal litijum-manganat baterije ima određene prednosti.Može osigurati da litijum ion pozitivne elektrode može biti u potpunosti ugrađen u ugljeničnu rupu negativne elektrode pod punim stanjem napunjenosti, umjesto da ima određene ostatke u pozitivnoj elektrodi poput litij kobalata, koji u određenoj mjeri izbjegava stvaranje dendriti.Stabilna struktura litijum-manganata čini njegovu oksidaciju mnogo nižom od one litij-kobalata.Čak i ako postoji vanjski kratki spoj (a ne unutrašnji kratki spoj), on u osnovi može izbjeći izgaranje i eksploziju uzrokovanu taloženjem metala litija.Litijum gvožđe fosfat ima veću termičku stabilnost i manji oksidacioni kapacitet elektrolita, tako da ima visoku sigurnost.
Slabljenje litijum jonske baterije se manifestuje slabljenjem kapaciteta i povećanjem unutrašnjeg otpora, a mehanizam unutrašnjeg prigušenja starenja uključuje gubitak pozitivnih i negativnih aktivnih materijala i gubitak raspoloživih litijum jona.Kada je materijal katode ostario i raspao, a kapacitet katode je nedovoljan, veća je vjerovatnoća da će se pojaviti rizik od evolucije litijuma iz katode.Pod uvjetom prekomjernog pražnjenja, potencijal katode prema litiju će porasti na iznad 3V, što je više od potencijala rastvaranja bakra, uzrokujući otapanje bakrenog kolektora.Otopljeni ioni bakra će precipitirati na površini katode i formirati bakrene dendrite.Bakarni dendriti će proći kroz dijafragmu, uzrokujući unutrašnji kratki spoj, što ozbiljno utiče na sigurnosne performanse baterije.
Osim toga, otpornost na prekomjerno punjenje starih baterija će se u određenoj mjeri smanjiti, uglavnom zbog povećanja unutrašnjeg otpora i smanjenja pozitivnih i negativnih aktivnih supstanci, što rezultira povećanjem džula topline tokom procesa prepunjavanja baterija.Pri manjem prekomjernom punjenju, mogu se pokrenuti nuspojave koje uzrokuju termički bijeg baterija.U smislu termičke stabilnosti, evolucija litijuma iz katode će dovesti do oštrog pada termičke stabilnosti baterije.
Jednom riječju, sigurnosne performanse stare baterije će biti znatno smanjene, što će ozbiljno ugroziti sigurnost baterije.Najčešće rješenje je opremanje sustava za pohranu energije baterije sistemom za upravljanje baterijom (BMS).Na primjer, baterije 8000 18650 koje se koriste u Tesla Model S mogu ostvariti praćenje različitih fizičkih parametara baterije u realnom vremenu, procijeniti status korištenja baterije i provesti online dijagnozu i rano upozorenje kroz svoj sistem upravljanja baterijom.U isto vrijeme, također može obavljati kontrolu pražnjenja i prethodnog punjenja, upravljanje balansom baterije i upravljanje temperaturom.
Vrijeme objave: Dec-02-2022